-
14例結直腸癌肝轉移患者樣本中發現治療新靶點——CTSD
發布時間: 2025-11-28 點擊次數: 12次結直腸癌肝轉移的困境
結直腸癌肝轉移是結直腸癌zui常見的遠處轉移形式,約15%-25%患者在初診時即合并肝轉移,約50%患者病程中發生肝轉移,其中約20%為同時性轉移(確診時即存在),30%為異時性轉移(術后隨訪出現)。 肝臟作為結直腸癌血行轉移最主要的靶器官,通過門靜脈系統形成轉移病灶。 手術切除原發灶及轉移灶仍是wei一gen治手段,但80%-90%的肝轉移灶初始無法gen治性切除。
近日,北京大學人民醫院胃腸外科申占龍教授、葉穎江教授和中國ke學院生物物理研究所李巖教授合作,在國際quan威期刊Advanced Science發表研究論文N-glycosylation modification of CTSD affects liver Metastases in colorectal cancer。該研究指出糖蛋白—組織蛋白酶D(CTSD)有望成為結直腸癌肝轉移的靶向治療靶點。

N-糖蛋白質組學實現結直腸肝轉移靶點
研究者分析了來自14例結直腸癌肝轉移患者的14對配對的原發灶和轉移灶癌組織:檢測到139個N-糖基化蛋白,185個N-糖基化修飾位點,共計490個完整結構的N-糖肽和71個糖基。差異分析發現組織蛋白酶D (CTSD) 263殘基上

N-糖基化修飾改變CTSD的折疊位置、穩定性和功能活性
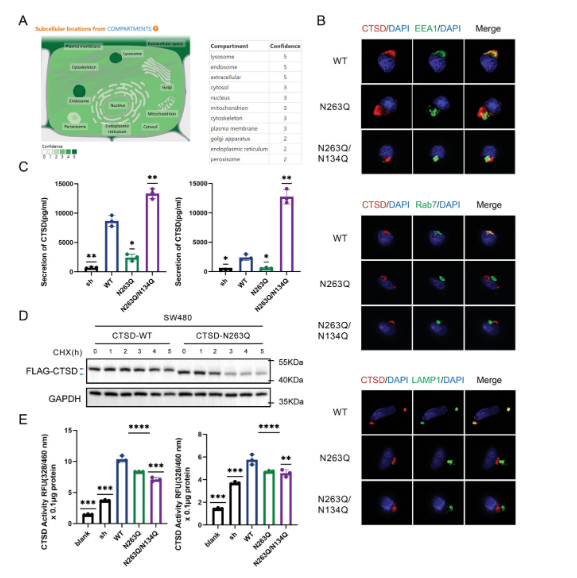
CTSD在CTSD N263Q和CTSD N263Q/N134Q細胞中不能與內體和溶酶體標記共定位(圖4B)。也就是說,下調CTSD殘基263的N-糖基化修飾水平可能會抑制其向SW480細胞內核內體和溶酶體的轉運。與CTSD WT細胞相比,部分缺失N-糖基化修飾的CTSD N263Q細胞的CTSD分泌量減少,而缺失N-糖基化修飾的CTSD N263Q/N134Q細胞的CTSD分泌量增加。因此,由于CTSD殘基263的N-糖基化修飾缺失,CRC細胞不能分泌CTSD。
此外,與CTSD WT細胞相比,環己酰亞胺處理3 h后,CTSD N263Q細胞中CTSD的數量明顯減少,說明CTSD在263殘基處的N-糖基化修飾影響了其穩定性。CTSD N263Q細胞和CTSD N263Q/N134Q細胞的CTSD熒光值低于CTSD WT細胞(圖4E)。具體來說,降低CTSD殘基134和263的N-糖基化修飾水平可能會降低其蛋白酶活性。綜上所述,CTSD殘基134和263的N-糖基化修飾可能會改變其折疊位置、穩定性和功能活性。
糖基化修飾的CTSD下游蛋白質篩選和鑒定
CTSD野生型細胞和CTSD N263Q細胞進行了比較蛋白質組分析。研究人員鑒定出在CTSD野生型細胞和CTSD N263Q細胞之間有差異表達的蛋白質共391個。鑒于CTSD的蛋白酶活性,研究人員對僅與CTSD野生型相互作用的蛋白質集和DEPs進行了交集分析。該分析共產生了8個候選分子:ACADM、PRDX3、ALDH2、EHHADH、DHCR7、TGFB1I1、IDH2和ALDH1A1。

STT3B和DDOST是CTSD的N-糖基轉移酶
免疫共沉淀富集與CTSD結合的蛋白,隨后通過質譜分析鑒定這些蛋白。分析結果顯示,235個蛋白與CTSD WT相互作用,191個蛋白與CTSD N263Q結合。在與CTSD WTwan全相互作用的45個蛋白中,DDOST(也稱為OST48)是wei一的N-糖基轉移酶,可能參與殘基263的N-糖基化修飾。最初的N-糖基轉移酶,也被稱為寡糖轉移酶復合物(OST),由多個蛋白質組成一個復合物。OST以OST-A和OST-B兩種形式存在,分別以STT3A和STT3B為催化亞基,分別負責初始N-糖基化。催化亞基能夠獨立完成N-糖基化加成過程。然而,在某些情況下,需要各種非催化亞基,如DDOST,在此過程中與底物形成穩定的配合物我們利用在線蛋白質組學數據庫CPTAC研究了STT3A、STT3B和DDOST在結腸癌組織和配對正常組織中的表達水平,發現這3種蛋白在結腸癌組織中表達上調。靶向敲除STT3A、STT3B和DDOST:當STT3B和DDOST的表達減少時,CTSD的分子量相對于陰性對照顯著降低,表明從N-糖基化向非N-糖基化轉變。這些發現表明,CTSD殘基263的N-糖基化可能受到DDOST的調控,STT3B可能是該位點的催化亞基。

CTSD的N-糖基化修飾調控ACADM/Ferroptosis軸促進CRC進展

研究總結
該研究表明CTSD的N-糖基化修飾顯著影響其分泌與活性,進而改變CRC細胞的侵襲/轉移能力并影響肝轉移形成。CTSD糖基化既可能作為預后/診斷生物標志物,也為阻斷結直腸癌肝轉移提供了新的分子干預靶點。
- 下一篇:沒有了
- 上一篇:一種小鼠肺癌原位移植的方法





